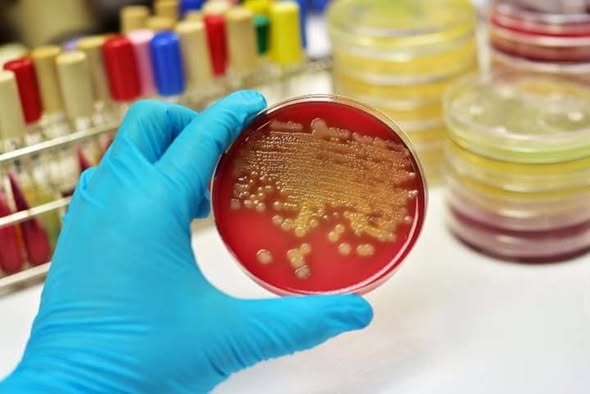
La coproculture est un examen bactériologique des selles visant à identifier les bactéries responsables d’infections digestives (diarrhées infectieuses, gastro-entérites, etc.). Voici le mode opératoire de la coproculture et la procédure pratique du déroulement de ce test au laboratoire.
Coproculture : Technique
1. Prélèvement des selles
- Utiliser un récipient stérile (pot à selles).
- Prélever une petite quantité de selles (éviter contamination avec urine ou eau).
- Si selles liquides : prélever 2–5 mL.
- Si selles solides : prélever une noix (~2–3 g).
- Transport rapide au laboratoire (≤ 2 heures).
- Si délai : conserver à 4°C ou utiliser un milieu de transport (type Cary-Blair).
2. Examen macroscopique
Observer :
- Couleur (normale, noire, rouge)
- Consistance (liquide, pâteuse, solide)
- Présence de mucus, sang ou parasites visibles
3. Examen microscopique:
- Préparation à l’état frais (solution saline)
- Recherche de :
- Leucocytes (infection bactérienne)
- Hématies
- bactéries mobiles : Campylobacter ..
- Parasites (œufs, kystes)
- levures
4. Ensemencement des milieux de culture
À l’aide d’une anse stérile :
Milieux classiques utilisés :
- Gélose MacConkey
→ sélectionne les entérobactéries et différencie lactose + / – - Gélose Hektoen
→ isolement de Salmonella et Shigella - Gélose SS
→ spécifique Salmonella/Shigella - Gélose XLD
→ différenciation entérobactéries pathogènes - (optionnel) gélose Campylobacter, si suspicion
Technique :
- Strier en quadrants pour isolement des colonies
En pratique on utilise uniquement le milieu spécifique SS.
5. Incubation
- Température : 35–37°C
- Durée : 18–24 h (jusqu’à 48 h si nécessaire)
- Atmosphère :
- Aérobie pour la plupart
- Microaérophile pour Campylobacter
6. Lecture des cultures
Observer :
- Aspect des colonies (taille, couleur, forme)
- Lactose + (rose sur MacConkey) vs lactose – (incolore)
- Production de H₂S (colonies noires)
Exemples :
- Salmonella → colonies incolores avec centre noir
- Shigella → colonies incolores sans H₂S
- Escherichia coli → colonies roses (lactose +)
7. Identification bactérienne
- Tests biochimiques :
- Galerie API 20E
- TSI, uréase, citrate…
- Identification automatisée possible (VITEK, MALDI-TOF)
8. Antibiogramme
- Réalisé si bactérie pathogène isolée
- Méthode :
- Diffusion sur disque (Kirby-Bauer)
- Permet de guider le traitement antibiotique
9. Interprétation
- Présence ou absence de bactéries pathogènes
- Corrélation avec les symptômes cliniques
- Certaines bactéries peuvent être commensales → donc prudence
Points importants
- Éviter prélèvement après antibiothérapie (faux négatifs)
- Prélèvements répétés parfois nécessaires
- Recherche ciblée selon contexte (voyage, épidémie…)



AWC CANADIAN PHARMACY canada pharmacy without prescription Cheap pharmacy viagra – Canada Pharmacy Online No prescription sky pharmacy online 24 hour cialis Orthopaedic Division of the Canadian Physiotherapy Association (CPA) How Much Does Celebrex Cost – USA Online Prices! Celebrex. Canadian Drugstore: DrugsPick – Buy Viagra, Cialis, Levitra Online non prescription india pharmacy Strattera Buy Viagra Online ::: Canadian Pharmacy. Lowest price.